A atividade a seguir foi vivenciada em um segundo ano do ensino médio em uma escola estadual do Rio de Janeiro. Trata-se da medição do pH de diferentes substâncias no PHET. Você pode acessar o simulador que utilizei clicando aqui. O cálculo do pH está diretamente ligado aos logaritmos e no site Brasil Escola encontrei as informações de que precisava para integrar a Matemática à Química em minha aula. Você pode acessar a matéria consultada clicando aqui.
Explorando
Iniciei a aula online explorando o aplicativo supracitado e pedi aos estudantes que observassem o pH medido e o valor da concentração de H3O+ registrado.
Comecei com a medição do pH do vômito.
Aqui, eles observaram que o valor da concentração de H3O+ era 1x 10-2 moL-1 e que o pH medido era 2.
Logo após, mostrei a medição do pH do ácido de bateria.
Aqui, eles observaram que o valor da concentração de H3O+ era 1x10-1 moL-1e que o pH medido era 1.
Logo após, mostrei a medição do pH da água.
Aqui, eles observaram que a concentração de era mol/L e que o pH medido era 7.
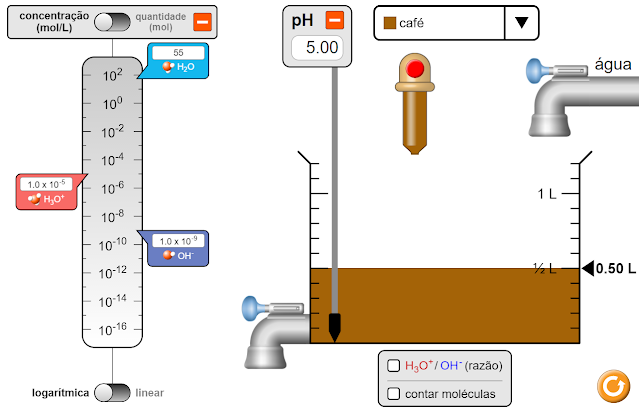
Na sequência, mostrei a medição do pH do café.
Aqui, eles observaram que o valor da concentração de H3O+ era 1x10^10-5 moL-1 e que o pH medido era 5.
A esta altura da exploração eles já haviam percebido que o pH estava ligado ao expoente da base 10, que se o expoente fosse -5 o pH era 5 (café), se o expoente fosse -1 o pH era 1(ácido de bateria), se o expoente fosse -2 0 pH era 2(vômito) e se o pH fosse -7 o pH era 7 (água). Observe que só utilizei valores de pH inteiros.
Atenção!
Se eu utilizasse uma substância cujo pH não fosse inteiro, cálculos adicionais seriam necessários, então, deixei investigações de casos como este para um momento posterior. Adiante você encontra um exemplo de medição de um pH não inteiro e de seu cálculo.
Desvendando o mistério
Após esta investigação era chegado o momento de mostrar a relação do logaritmo com a medição do pH. Comecei explicando o que era pH.
fonte: https://brasilescola.uol.com.br/quimica/calculos-envolvendo-ph-solucoes.htm
Depois, apresentei a fórmula que relaciona pH ao logaritmo.
A partir desta equação logarítmica chegamos na relação que eles perceberam no simulador PHET.
Voltando ao café
Mostrei então como a fórmula que tínhamos visto era aplicada e os alunos a relacionaram com o que tinham percebido na exploração.
Considerações finais
Agradecimentos
A autora
Daniela Mendes Vieira da Silva é doutora pelo programa de pós graduação em ensino de Matemática da UFRJ, professora adjunta do departamento de Matemática da FFP/UERJ, coordenadora geral do projeto de extensão LEM FFP UERJ ITINERANTE e do projeto de pesquisa, fomentado pela FAPERJ, Matemática e Física na mala. Orientadora do programa Residência Pedagógica, Matemática-FFP/UERJ da CAPES. É também líder do grupo de pesquisa em aprendizagem e ensino de Matemática da FFP-UERJ (GPAEM-FFP) e coordenadora do Programa de Mestrado Profissional em Matemática em Rede Nacional (Profmat) na FFP/UERJ.